Primeira imagem de uma proteína individual
Redação do Diário da Saúde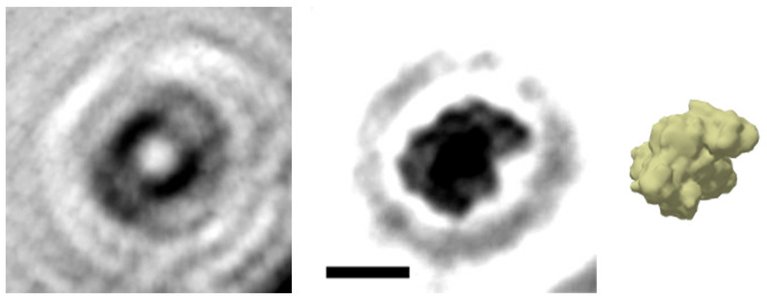
[Imagem: Jean-Nicolas Longchamp/University of Zurich]
Foto de uma proteína
Embora falem o tempo todo nas proteínas e em seus dobramentos, esta é a primeira imagem razoavelmente clara que os cientistas já obtiveram de uma molécula de proteína dobrada.
As proteínas são as ferramentas da vida, mas as coisas podem começar a dar errado quando seus dobramentos não saem como esperado.
Conhecer a estrutura de cada proteína é de interesse não só para os biólogos que querem entender como funciona um organismo, mas também para os médicos e farmacêuticos, que precisam saber como as proteínas são construídas, como elas interagem com outras proteínas e com moléculas menores, e como esses pontos de ligação mudam conforme a proteína desempenha suas funções.
Com a possibilidade de vê-las diretamente, passa a ser possível examinar moléculas individuais para saber tudo isto e mais - por exemplo, como elas interagem com potenciais medicamentos, para tentar corrigir seu comportamento quando as coisas começam a dar errado.

[Imagem: Tatiana Latychevskaia /University of Zurich]
Holograma eletrônico
A primeira imagem da proteína dobrada foi possível graças a uma técnica de holograma eletrônico desenvolvida por uma equipe da Universidade de Zurique (Suíça) e do Instituto Max Planck (Alemanha). Embora a geração de hologramas seja bem conhecida, foi necessário desenvolver uma técnica com elétrons de energia muito baixa, para não danificar a proteína que está sendo observada.
Os métodos atuais, tais como análise por raios X e a microscopia crioeletrônica, exigem que as biomoléculas estejam cristalizadas ou que se use uma grande quantidade de cada proteína.
O problema é que muitas proteínas não crescem na forma de cristais e, quando se usam valores médios nem sempre é possível detectar diferenças entre várias conformações, isto é, variantes estruturais da biomolécula. E são precisamente essas variações que são importantes na busca de novos fármacos, uma vez que as proteínas assumem várias conformações quando desempenham suas funções.
| Ver mais notícias sobre os temas: | |||
Nanotecnologia | Desenvolvimento de Medicamentos | Alimentação e Nutrição | |
| Ver todos os temas >> | |||
Melhor programa de treinamento é mais simples que você imagina e dispensa academia
Sete dias de meditação reprogramam seu cérebro
Ruído rosa: Sons para dormir podem prejudicar memória e desenvolvimento cerebral
Timo saudável reduz mortalidade em até 92%
Alzheimer: Não é aglomeração de amiloides ou tau, é a competição entre elas
Basta esticar ou massagear a pele para alertar o sistema imunológico
Da especulação à ciência: Seres humanos são seres musicais
Sua reação aos próprios erros indica seu risco de ansiedade e depressão
Ficar ofegante poucos minutos por dia reduz risco de oito doenças
Nova teoria tenta explicar consciência e nossa compreensão do tempo
Conceito budista da Rede de Indra como terapia para o mundo digital
Ultrassom cria luz no interior do corpo para aplicações médicas
Emoções dos entes queridos influenciam processo de luto
Proximidade de usinas nucleares aumenta mortalidade por câncer
Terapia gênica devolve audição a pessoas que nasceram surdas
Delegar tarefas à inteligência artificial aumenta desonestidade drasticamente
Ficar ofegante poucos minutos por dia reduz risco de oito doenças
DNA está em constante movimento, e isso pode explicar o câncer
Como nosso corpo sente o frio - e por que o mentol dá o mesmo efeito
Sua reação aos próprios erros indica seu risco de ansiedade e depressão
Vacina do Butantan contra dengue grave tem 89% de proteção
Brasil tem primeiras mortes por febre oropouche no mundo
Censo 2022: Por que várias cidades brasileiras tiveram diminuição da população?
Brasil tem primeiro caso de gripe aviária em aves domésticas
Brasil decreta emergência zoossanitária devido à gripe aviária
Proibido o uso de animais em pesquisas de cosméticos e higiene pessoal
A informação disponível neste site é estritamente jornalística, não substituindo o parecer médico profissional. Sempre consulte o seu médico sobre qualquer assunto relativo à sua saúde e aos seus tratamentos e medicamentos.
Copyright 2006-2026 www.diariodasaude.com.br. Todos os direitos reservados para os respectivos detentores das marcas. Reprodução proibida.


