Rumo a uma terapia gênica para tratamento do autismo
Com informações da Agência Fapesp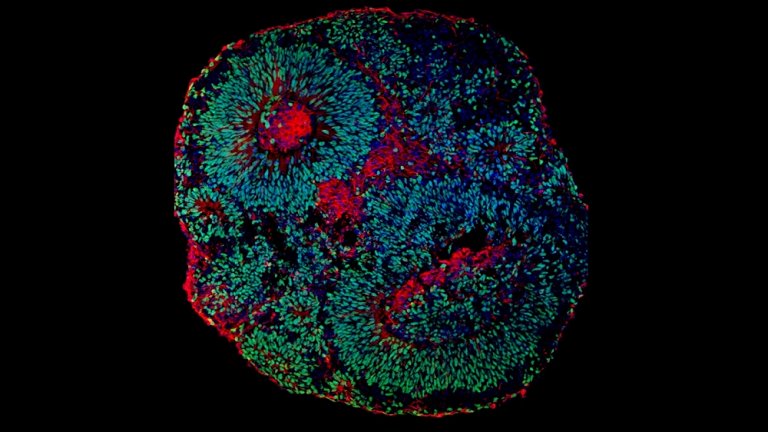
[Imagem: Fábio Papes/Unicamp]
Síndrome de Pitt-Hopkins
Um grupo liderado por cientistas da Universidade Estadual de Campinas (Unicamp) e da Universidade da Califórnia San Diego, nos Estados Unidos, desvendou o mecanismo causador da síndrome de Pitt-Hopkins, uma disfunção neuropsiquiátrica que tem características de transtorno do espectro autista (TEA).
Além disso, os pesquisadores conseguiram reverter a evolução da síndrome em modelos de laboratório, abrindo novas possibilidades de tratamento.
"Para a maioria dos casos de TEA, não se sabe qual gene causa a condição quando mutado. Assim é também para a maioria das doenças neuropsiquiátricas, como esquizofrenia, depressão e transtorno bipolar. A síndrome de Pitt-Hopkins, por sua vez, tem como origem uma mutação no gene TCF4. Mas, até então, não eram conhecidos seus mecanismos moleculares, ou seja, o que há de diferente nas células do sistema nervoso dos pacientes com a mutação," destacou o professor Fábio Papes, um dos coordenadores do estudo.
Os cientistas testaram maneiras de interferir na evolução do quadro e conseguiram reverter os efeitos causados pela mutação. O sucesso obtido nos experimentos abre caminho para o desenvolvimento tanto de medicamentos como de uma terapia gênica.
A síndrome de Pitt-Hopkins é caracterizada por déficit cognitivo, atraso motor profundo, ausência de fala funcional e anormalidades respiratórias, entre outros. Foi descrita em 1978, mas seu gene causador ficou conhecido apenas em 2007. Estima-se que a mutação no gene TCF4 ocorra em um a cada 35 mil nascimentos.
Minicérebros
Como esta síndrome não se desenvolve em camundongos da mesma maneira que em humanos, o estudo em animais é inviável. Por isso, os pesquisadores usaram os chamados organoides cerebrais, um aglomerado de células humanas que cresce no laboratório e se assemelha a uma miniatura de cérebro em desenvolvimento, mas sem vascularização e com menos tipo celulares.
"O organoide cerebral é um modelo mais representativo do que qualquer outro para estudar disfunções do sistema nervoso central. Nesse caso, a célula obtida é do próprio paciente. Além disso, o organoide é tridimensional, portanto, seu funcionamento é mais próximo da realidade do que o de células cultivadas em placas, que crescem em apenas duas dimensões," explicou Papes.
Os organoides foram gerados a partir de biópsias da pele de portadores da síndrome, obtidas de pacientes recrutados na Unicamp e nos Estados Unidos, além de seus pais, que serviram como controle.
As células foram cultivadas para extrair os chamados fibroblastos, que são transformados em células-tronco pluripotentes, que, por sua vez, podem gerar muitos tipos de células humanas. Nesse caso, elas deram origem a neurônios, células progenitoras do sistema nervoso central e organoides cerebrais.
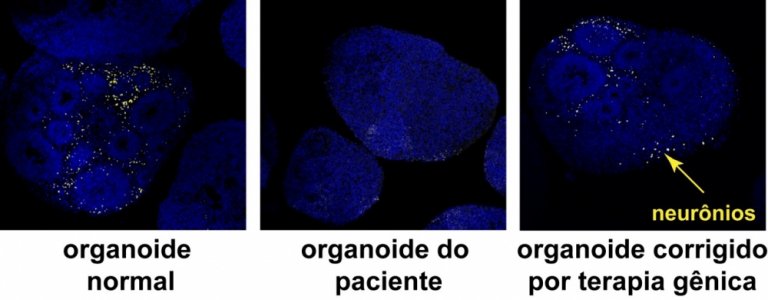
[Imagem: Fábio Papes/Unicamp]
Cérebro artificial e cérebro de verdade
Enquanto as células dos pais dos pacientes formaram organoides que se desenvolviam normalmente, as dos portadores da síndrome cresciam menos, como resultado da menor replicação das células causada pela mutação e de um prejuízo da própria neurogênese. Ou seja, a geração de neurônios foi prejudicada por conta da mutação.
Além disso, os neurônios dos organoides com a mutação no TCF4 existiam em menor número e tinham menor atividade elétrica em comparação aos de organoides-controle. Como a comunicação entre essas células é feita a partir de impulsos elétricos, sem os quais elas não podem exercer suas funções, esta descoberta pode explicar muitas características clínicas dos pacientes.
Os resultados foram semelhantes aos obtidos em tecidos do cérebro de um paciente com a condição, que faleceu por outras razões, o que reforça as conclusões obtidas com os organoides. O estudo foi o primeiro de que se tem notícia a estudar o cérebro de uma pessoa com síndrome de Pitt-Hopkins.
"O acesso ao cérebro post-mortem foi essencial para validarmos alguns dos resultados obtidos com os organoides cerebrais. O fato de termos visto características semelhantes entre o organoide criado em laboratório e o cérebro mostra o quão relevante é essa tecnologia," afirmou Alysson Muotri, membro da equipe.
Terapia gênica
Uma vez observadas as alterações causadas pela mutação no gene TCF4, os pesquisadores buscaram maneiras de corrigi-la e, assim, realizar o que eles chamam de uma prova de conceito do que seria um tratamento.
Três intervenções foram testadas. A primeira utilizou a técnica de edição gênica conhecida como CRISPR-Cas9 - cujas criadoras ganharam o Prêmio Nobel de Química em 2020, e a segunda envolveu a inserção de uma cópia extra do gene, que passou a exercer normalmente as funções gênicas, compensando a cópia mutada.
Os organoides que sofreram as intervenções passaram a crescer normalmente e tiveram um aumento da proliferação das células progenitoras, que no cérebro dão origem a diferentes tipos de célula, inclusive neurônios.
Uma terceira intervenção foi a aplicação de uma droga usada em estudos com células tumorais. Conhecida pela sigla CHIR99021, ela ativa uma via de sinalização celular conhecida como Wnt, muito estudada no contexto do câncer e que os autores descobriram ser alterada também por mutações no gene TCF4.
Em células e organoides disfuncionais tratados com a droga houve melhora em alguns indicadores moleculares e aumento de tamanho (no caso dos organoides). Os resultados abrem caminho para o desenvolvimento de medicamentos similares que possam tratar a disfunção, uma vez que a CHIR99021 ainda não pode ser utilizada em seres humanos.
A pesquisa agora deve avançar para estudos pré-clínicos e clínicos. Os pesquisadores fecharam parceria com uma empresa especializada em terapia gênica, que está licenciando a tecnologia usada nos experimentos para que futuramente possa ser testada em humanos.
Artigo: Transcription Factor 4 loss-of-function is associated with deficits in progenitor proliferation and cortical neuron content
Autores: Fabio Papes, Antonio P. Camargo, Janaina S. de Souza, Vinicius M. A. Carvalho, Ryan A. Szeto, Erin LaMontagne, José R. Teixeira, Simoni H. Avansini, Sandra M. Sánchez-Sánchez, Thiago S. Nakahara, Carolina N. Santo, Wei Wu, Hang Yao, Barbara M. P. Araújo, Paulo E. N. F. Velho, Gabriel G. Haddad, Alysson R. Muotri
Publicação: Nature Communications
Vol.: 13, Article number: 2387
DOI: 10.1038/s41467-022-29942-w
| Ver mais notícias sobre os temas: | |||
Genética | Comportamento | Cérebro | |
| Ver todos os temas >> | |||
Comer ovos está associado a um menor risco de doença de Alzheimer
Teste simples de senta-levanta por 30s prevê o quão bem você envelhecerá
Humanos podem regenerar tecidos e membros? Ciência diz que é muito provável
Creatina: do esporte ao cérebro, o que a ciência realmente diz sobre o suplemento
Dieta de 4 semanas pode lhe tornar biologicamente mais jovem
Cientistas revelam o melhor exercício para aliviar a dor da artrite no joelho
Envelhecimento cerebral é revertido com um spray nasal
Composto vegetal raro contra o câncer acaba de ser decifrado
Descoberta acidental mostra DNA quebrando as regras da vida
O complexo sentido de "religião" no Japão
Pernilongos aprendem a associar repelente de insetos a fonte de alimento
Homens ou mulheres são mais bonitos? As mulheres decidem o resultado
Seus amigos são mais cínicos do que você?
Minirrobô cirurgião 5 em 1 tem tamanho de um grão de arroz
Chip brasileiro integra múltiplos sensores para análises clínicas em alta velocidade
Suplementos de cálcio e vitamina D não previnem fraturas e quedas em idosos
Gosto de você, mas não fique tão perto
Órgãos criados em laboratório são transplantados com sucesso
Tatuagem inteligente detecta câncer de pele antes que ele apareça
Medo e ansiedade ainda são úteis aos humanos? A resposta irá lhe surpreender
Vacina do Butantan contra dengue grave tem 89% de proteção
Brasil tem primeiras mortes por febre oropouche no mundo
Censo 2022: Por que várias cidades brasileiras tiveram diminuição da população?
Brasil tem primeiro caso de gripe aviária em aves domésticas
Brasil decreta emergência zoossanitária devido à gripe aviária
Proibido o uso de animais em pesquisas de cosméticos e higiene pessoal
A informação disponível neste site é estritamente jornalística, não substituindo o parecer médico profissional. Sempre consulte o seu médico sobre qualquer assunto relativo à sua saúde e aos seus tratamentos e medicamentos.
Copyright 2006-2026 www.diariodasaude.com.br. Todos os direitos reservados para os respectivos detentores das marcas. Reprodução proibida.


